蓄電池の基本構造
蓄電池が電気を蓄えて何度も利用できる仕組み
蓄電池は、蓄えていた電気を使ってしまえば、再び充電をすることで、また電気が使用できるようになる装置です。
では、蓄電池は、どのようにして電気を蓄えて(充電という)、その蓄えた電気を必要に応じて取り出して(放電という)利用できるのでしょうか?
蓄電池は電気エネルギーを化学エネルギーに、そして化学エネルギーを電気エネルギーに双方向に電気で化学反応を起こすことで蓄電・放電させることができる仕組みになっています。
尚、蓄電池の放電・充電は、このように書くと無限にできるように思えますが、実際は有限回数しかできず、それが蓄電池の寿命となります。蓄電池の種類ごとにその回数は異なります。
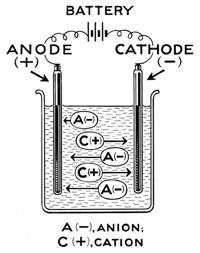
その詳細な仕組みは、たくさんある蓄電池の種類によって異なりますが、簡単に基本的な仕組みを説明すると、プラスとマイナスの電極に、それぞれに適したリチウムやニッケル、鉛、炭素、カドミウムなどの金属を使用し、それを電解液に浸すことで起こる電気化学反応(酸化還元反応)を利用して蓄電しています。
一次電池は、放電時に発生する化学反応が進むと、ある時点でそれ以上は放電できなくなり、電気を利用できなくなりますが、蓄電池は電極と電解液に適切な材料を選択することで、放電時に起きている化学反応と逆の化学反応を電気を使って起こすことで充電させることができます。
そのため電気エネルギーが化学エネルギーに変換されて再び蓄電されるので、また電気を使用することができるようになります。
蓄電池の基本構造
蓄電池は、簡単にいうと正極(プラスの電極)、負極(マイナスの電極)と電解液でできており、図式化すると以下のように単純化されます。


蓄電池には、たくさんの種類がありますが、この3つにどのような材料を使うかで、蓄電池の性能・特徴が決まります。
また、新しい材料を見つけ、組み合わせることで、より性能の良い蓄電池ができるようになります。
その開発は、大学や企業が行い、研究・開発し実用化を目指しています。
実用化に至っていない蓄電池を含めると非常にたくさんの種類の蓄電池があります。
主な蓄電池に使われている材料の例
| 蓄電池の種類 | 正極 | 電解質 | 負極 |
|---|---|---|---|
| 鉛蓄電池 | 二酸化鉛 | 希硫酸 | 鉛の合金 |
| リチウムイオン電池 | リチウム金属酸化物 | 有機溶媒 | 黒鉛(炭素) |
| ニッケル・カドミウム電池 | ニッケル酸化物 | アルカリ水溶液 | カドミウム |
| ニッケル・水素電池 | ニッケル酸化物 | アルカリ水溶液 | 水素吸蔵合金 |